Vacunas: más estudios, una buena noticia para chicos, embarazadas y mayores de 65 años

WASHINGTON.- Mientras los países corren para aprobar y distribuir las vacunas contra el Covid-19, los investigadores van acumulando saber e información sobre las mismas. Las vacunas de Oxford/AstraZeneca, Moderna, Johnson & Johnson y Pfizer-BioNTech, todas con autorización de emergencia en muchos países, habían sido sometidas al riguroso referato de sus pares científicos. (China y Rusia no han hecho públicos gran parte de los datos de sus vacunas.)
Por diversas razones, sin embargo, aquellas primeras rondas de ensayos excluyeron explícitamente a los niños, las embarazadas, las madres de lactantes, y en algunos casos los mayores de 65 años estuvieron muy subrepresentados. De hecho, algunos gobiernos todavía no han autorizado la aplicación de vacunas a esos grupos poblacionales menos estudiados.
¿Por qué no lo usa? El avión dorado de Donald Trump, abandonado
Pero esa situación está a punto de cambiar: para lograr la aprobación generalizada y permanente de los organismos reguladores, los laboratorios han ampliado los estudios y ensayos clínicos de sus vacunas.
Así avanza la investigación de los efectos en estos grupos poblacionales:
Chicos
Los científicos saben que los chicos son menos propensos a desarrollar un caso grave de Covid-19. En parte, por eso hasta ahora las vacunas no se habían testeado ni aprobado para menos de 16 o 18 años, según la vacuna. Los niños además necesitan de una dosis específica, así que no pueden ser estudiados en el mismo ensayo que los adultos.
Este martes, sin embargo, los niños de entre 6 meses y 12 años empezaron a recibir su dosis en un ensayo dirigido por el laboratorio Moderna sobre un total de 6750 chicos. Dentro de ese grupo, los de mayor edad serán vacunados primero, y los investigadores luego avanzaron con los menores de 6 años.
Moderna y el gigante farmacéutico norteamericano Pfizer en sociedad con la alemana BioNTech ya lanzaron ensayos en adolescentes mayores de 12 años, mientras que la sueco-británica AstraZeneca y su socia la Universidad de Oxford vienen estudiando desde febrero el efecto de su vacuna en niños mayores de 6 años. La norteamericana Johnson & Johnson también anunció que planea dos ensayos clínicos en grupos de menores.
La semana pasada, Israel informó que su ensayo con la vacuna Pfier-BioNTech sobre 600 adolescentes de entre 12 y 16 años no había revelado efectos adversos hasta el momento.
Sin embargo, pasarán meses hasta que los estudios hayan sido completados. Robert Frenck, investigador en jefe del ensayo de la vacuna de Pfizer en el Hospital de Niños de Cincinnati dijo el mes pasado que los niños pequeños de Estados Unidos tendrán que esperar al año que viene para ser vacunados. Los científicos todavía tienen que determinar como incluir una nueva vacuna en el ya cargado calendario de vacunación de la primera infancia.
Embarazadas y madres que amamantan
Cuando salieron las primeras vacunas, muchos gobiernos desaconsejaron la inoculación de embarazadas, madres que amamantan, o mujeres que tuvieran planeado ser madres en lo inmediato. Los entes reguladores adujeron entonces la falta de datos, ya que esos grupos poblacionales habían sido excluidos de los ensayos clínicos, debido a su mayor riesgo.
Es normal excluir a las embarazadas de los ensayos clínicos, aunque algunos expertos sanitaristas les reclamaron a los investigadores que en el caso del coronavirus reconsideraran ese abordaje. A medida que los científicos aprendieron más del virus y las vacunas, su recomendación inicial empezó a cambiar.

Los entes reguladores de muchos países ya permiten la inoculación de embarazadas y mujeres que amamantan, aunque les aconsejan una consulta médica previa. En Israel, las autoridades fueron aún más lejos, alentando a las embarazadas a vacunarse, tras un rebrote de las internaciones y complicaciones en el embarazo atribuidas a las nuevas variantes supercontagiosas del virus.
Coronavirus: las dos cifras récord que elevan la alarma en Chile
El mes pasado, Pfizer-BioNTech anunció el lanzamiento de un estudio global de su vacuna en 4000 embarazadas sanas mayores de 18 años.
“Las mujeres embarazadas tienen mayor riesgo de complicaciones y de desarrollar Covid-19 grave, así que es fundamental desarrollar una vacuna segura y eficaz para ese grupo”, dijo en ese momento William Gruber, vicepresidente de investigación y desarrollo clínico de Pfizer a través de un comunicado.
Además de responder las dudas sobre la seguridad de las vacunas, los científicos esperan descubrir si una mujer embarazada vacunada puede transmitirle inmunidad a su feto. Un estudio a pequeña escala realizado en Israel sobre 10 madres de lactantes vacunadas reveló que la leche materna contenía anticuerpos contra el coronavirus. El jueves, investigadores estadounidenses informaron el primer caso conocido a nivel nacional de una madre vacunada que dio a luz a un bebé con anticuerpos contra el coronavirus.
Mayores de 65 años
El 30 de diciembre, Gran Bretaña se convirtió en el primer país que autorizó el uso de emergencia de la vacuna de Oxford-AstraZeneca, y pocos días más tarde, el personal médico empezó a inocular a los adultos mayores.
Muchos otros países que empezaron a autorizar la vacuna, sin embargo, no la habilitaron para los mayores de 65 años. Al revisar los datos de los ensayos clínicos de AstraZeneca, los entes reguladores de algunos países concluyeron que los adultos mayores estaban subrepresentados en los estudios. En Indonesia, por ejemplo, el gobierno aprobó la vacuna de AstraZeneca, pero solo para los menores de 60 años: el presidente indonesio calificaba para recibirla, el vicepresidente no.
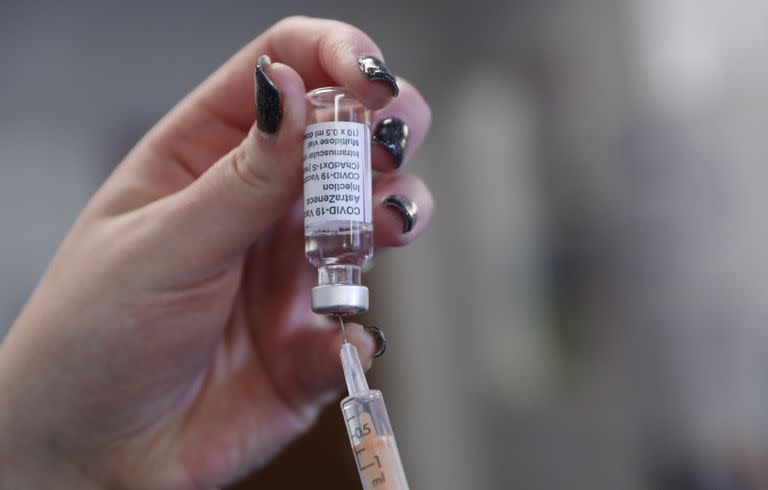
En las semanas pasadas desde entonces, muchos países cambiaron sus directivas. El martes, Canadá fue el más reciente en autorizar el uso de la vacuna en mayores de 65, revirtiendo así su lineamiento previo. Y los reguladores canadienses no tuvieron necesidad de recurrir a nuevos ensayos clínicos: les bastó con revisar los datos recolectados en Gran Bretaña, donde la vacuna es ampliamente utilizada desde hace dos meses.
“Ya contamos con evidencia del mundo real que nos llega del Reino Unido, donde la vacuna de AstraZeneca se aplica a los mayores de 65 sin ningún problema”, dice el comunicado del Comité Asesor en Inmunizaciones de Canadá. “La evidencia demuestra la elevada seguridad y efectividad de la vacuna de AstraZeneca en adultos mayores.”
De hecho, las nuevas medidas de algunos países representan un giro de 180 grados: la vacuna de AstraZeneca para los adultos mayores, pero no para los jóvenes. El viernes, el comité asesor de Francia recomendó que los menores de 55 años no reciban la vacuna de AstraZeneca, debido a las dudas sobre la formación de coágulos sanguíneos. Algunos estados de Alemania están aplicando políticas similares.
Por otro lado, está previsto que el primer ministro británico Boris Johnson, de 56 años, reciba el viernes su primera dosis de AstraZeneca.
The Washington Post
(Traducción de Jaime Arrambide)

 Yahoo Noticias
Yahoo Noticias 
