5 cosas que debe saber sobre la nueva vacuna RSV
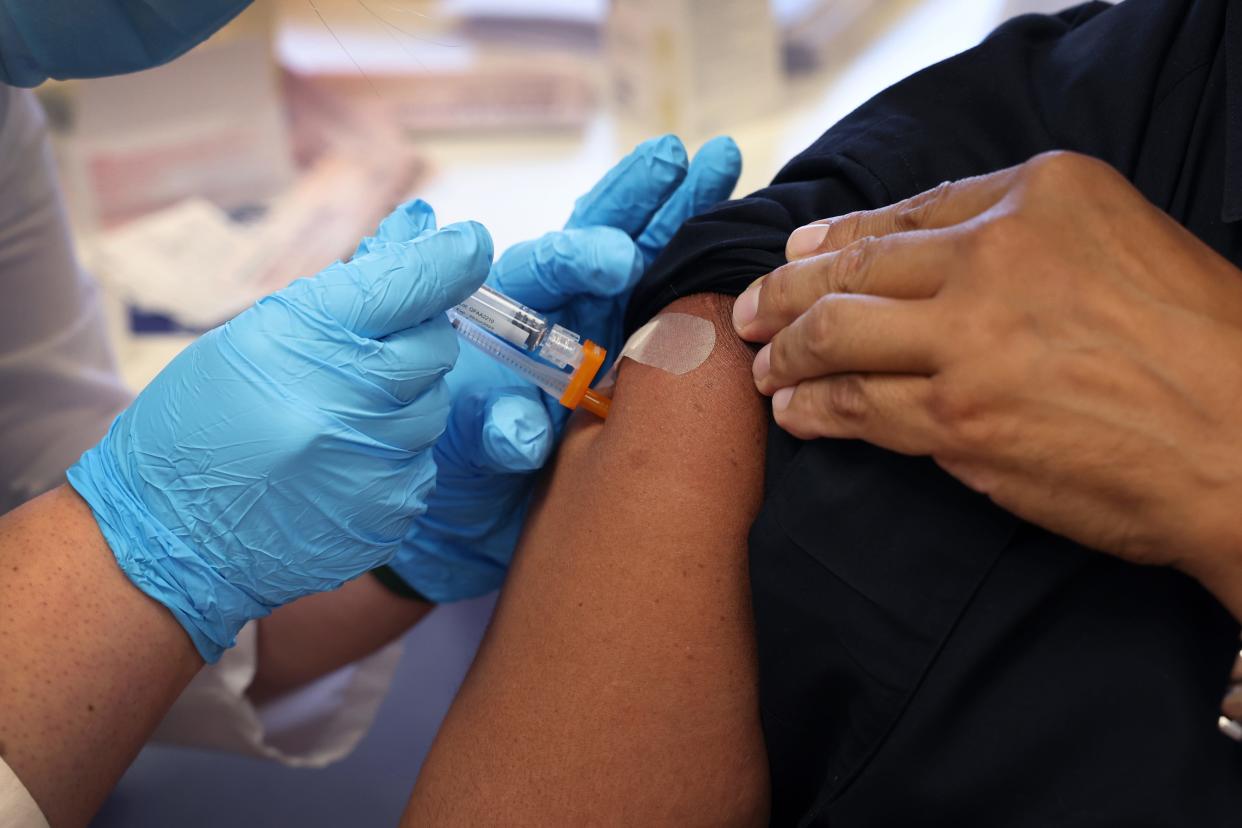
La Administración de Drogas y Alimentos de Estados Unidos (FDA por sus siglas en inglés) aprobó este mes una nueva vacuna para prevenir el virus sincitial respiratorio (RSV por sus siglas en inglés) para personas mayores de 60 años de edad.
El RSV es un virus altamente contagioso que se transmite por el aire y que infecta los pulmones y, a veces, causa otras enfermedades respiratorias, como neumonía y bronquiolitis, que pueden poner en peligro la vida de los adultos mayores.
Los Centros para el Control de Enfermedades (CDC por sus siglas en inglés) estiman que entre 60 mil y 160 mil adultos mayores son hospitalizados cada año debido al RSV, y entre 6 mil y 14 mil muertes se atribuyen al RSV en adultos mayores de 65 años.
La aprobación de la vacuna, Arexvy, se produjo después de que se recopilaran datos durante un estudio clínico en curso de tres años de aproximadamente 25 mil adultos de 60 años o más en Estados Unidos e internacionalmente.
La temporada de RSV generalmente se extiende desde diciembre hasta febrero, aumentando en el otoño y disminuyendo a principios de la primavera.
La vacuna es un gran avance que la gente ha estado esperando durante unos 60 años, dijo la Dra. Katie Sharff, jefa de enfermedades infecciosas de Kaiser Permanente Northwest.
“Definitivamente existe la necesidad de tener una capa adicional de protección contra el RSV”, mencionó Sharff.
¿Quién puede vacunarse y cuándo puede hacerlo?
La vacuna solo estará disponible para personas mayores de 60 años.
Las personas que deseen vacunarse contra el RSV pueden hacerlo en algún momento del otoño. No estará disponible hasta entonces porque un comité de los CDC está brindando recomendaciones sobre las mejores prácticas médicas en distribución y uso.
¿Se necesitará más de una vacuna?
Actualmente, Arexvy es una vacuna de una sola dosis.
A medida que avanza el estudio clínico de 3 años y se sigue estudiando la eficacia de la vacuna, se podría recomendar otra dosis, señaló Sharff.
¿Qué tan efectiva y segura es la vacuna?
En el primer año del ensayo principal, Arexvy tuvo una eficacia del 83 por ciento en la reducción del riesgo de enfermedad de las vías respiratorias inferiores causada por el RSV y del 94 por ciento en la prevención de enfermedades graves.
Los efectos secundarios informados con mayor frecuencia por los participantes del estudio fueron dolor en el lugar de la inyección, fatiga, dolor muscular, dolor de cabeza y rigidez y dolor en las articulaciones.
Entre los aproximadamente 25 mil participantes del ensayo clínico, 10 que recibieron la vacuna y cuatro que recibieron un placebo informaron de fibrilación auricular, o ritmo cardíaco rápido e irregular, dentro de los 30 días.
La vacunación ha sido aprobada como segura para su uso por la Administración de Drogas y Alimentos, y el riesgo de efectos secundarios, como la fibrilación auricular, continuará siendo revisado en un estudio posterior a la comercialización.
¿Se puede recibir otras vacunas al mismo tiempo?
No se sabe si la vacuna RSV se puede administrar junto con las vacunas contra el COVID-19 y la influenza.
Los CDC revisarán esto en los próximos meses y se proporcionarán recomendaciones médicas para la administración conjunta de Arexvy antes del lanzamiento de la vacuna, apuntó Sharff.
¿Qué pasa con los niños y los bebés?
En bebés y niños, la contracción del RSV también puede poner en peligro la vida, especialmente en bebés prematuros, menores de seis meses y niños con sistemas inmunitarios debilitados, trastornos neuromusculares y enfermedad pulmonar crónica, según los CDC.
RSV es la causa de muerte hasta para 300 niños menores de cinco años cada año en Estados Unidos.
La farmacéutica Pfizer ha desarrollado una vacuna para mujeres de entre 24 y 36 semanas de embarazo que pretende prevenir el RSV en los bebés. Esta vacuna aún no ha sido aprobada por la Administración de Drogas y Alimentos, por lo que aún no está disponible para el público.
En un ensayo clínico de la vacuna con casi 7 mil 400 participantes, se redujo el riesgo de enfermedad grave por RSV en bebés en un 82 por ciento dentro de los tres meses posteriores al nacimiento. Alrededor de los seis meses, la eficacia fue de alrededor del 69 por ciento.
Sydney Wyatt cubre desigualdades en el cuidado de la salud en Mid-Willamette Valley para el periódico Statesman Journal. Comuníquese con ella por correo electrónico SWyatt@gannett.com, por teléfono (503) 399-6613 o en Twitter @sydney_elise44.
La cobertura del Statesman Journal sobre las inequidades en la atención médica está financiada en parte por M.J. Murdock Charitable Trust, que busca fortalecer la base cultural, social, educativa y espiritual del noroeste del Pacífico a través de inversiones para el desarrollo de capacidades en el sector sin fines de lucro.
Traducción Alfredo García
This article originally appeared on Salem Statesman Journal: 5 cosas que debe saber sobre la nueva vacuna RSV

 Yahoo Noticias
Yahoo Noticias 
